PRODUCTOS SANITARIOS


.
REGLAMENTO MDR (EU) 2017/745
MDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2021
RD 192/2023
RD – ingles
entrada en vigor: 23 marzo 2023
«legacy» s/reglamento 2023/607
IIb(implante) y III -31 dic 2027
IIa, IIb(no implant) y I (ON) -31 dic 2028
sin fin periodo distribución
.
PRODUCTOS SANITARIOS IVD


.
REGLAMENTO IVDR (EU) 2017/746
IVDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2022
RD IVD
entrada en vigor: 2024?
«legacy»s/reglamento 2024/1860
clase D – 31 Dic 2027
clase C – 31 Dic 2028
clases B y As – 31 Dic 2029
sin fin periodo distribución
.
PROXIMA FORMACIÓN
REPETIMOS !!! 23 Abril ven a la formación «IMPACTO REGLAMENTO EN SECTOR OPTICA/AUDIOLOGIA» de FEDAO / AEO impartida por @Tecno_med en @optometria_cat
Dada la relevancia de los cambios en el sector debido al reglamento /EU) 2017/745 nos han pedido que repitamos la jornada en Barcelona.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
Organismos Notificados: IMQ ( ON num. 0051 ) nuevo ON con el reglamento MDR – Enhorabuena!!
Publicado primero el Decreto por el Ministerio della Salute y ahora en NANDO
IMQ ISTITUTO ITALIANO DEL MARCHIO DI QUALITÀ S.P.A.
Via Quintiliano, 43
20138 – MILANO – Italy
Phone : +39 02 50731
Email : info@imq.it
Website : www.imq.it
Notified Body number : 0051 read more…
Organismos Notificados: IMQ ( ON num. 0051 ) será en breve nuevo ON con el reglamento MDR – Enhorabuena!!
Publicado el Decreto por el Ministerio della Salute, ahora pendiente de su publicación en NANDO read more…
Curso «Expert3D Transversal Programme in Medical Image Postprocess, Training Professionals: 3D Printing to Research» 2019 liderado por la @SJDFormacion
Puedes ver mas información, programa, el cuadro docente e inscripción aquí
Colaboramos en:
• MODULE 1: Existing regulations and ethics in healthcare — profesores: Claire Murphy y Xavier Canals
FAQ UDI – ¿Cuando, donde, como ? EU – UDI según reglamentos MDR e IVDR
Organismos Notificados: DEKRA ( ON num. 0124 ) nuevo Organismo Notificado con el reglamento MDR – Enhorabuena!!
Tal y como ya os avanzamos tenemos nuevo ON para la MDR : DEKRA
DEKRA Certification GmbH
Handwerkstraße 15
70565 STUTTGART
Country : Germany
Phone : +49 711 / 7861 1947
Fax : +49 711 / 7861 3450
Email : medizinprodukte.certification.de@dekra.com
Website : www.dekra-certification.de
Notified Body number : 0124
podemos consultar aqui el scope : https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=notification.html&ntf_id=299688&version_no=15
Puntos que llaman la atención de las especificaciones comunes para reprocesado de productos sanitarios de un sólo uso
Una vez leídas las especificaciones comunes para el represado de productos sanitarios de un solo uso, os queremos comentar puntos que nos han llamado la atención. read more…
Nueva modificación de la EN ISO 13485:2016 Amd 1:2019 para incluir los anexos ZD (MDR) y ZE (IVDR)
A punto de publicarse la modificación de la EN ISO 13485:2016 (nótese que la ISO 13485:2016 no cambia) que incluye los anexos que establecen que requisitos no cubre la norma para el cumplimiento de los Reglamentos de productos sanitarios. Incluye la comparación con los requisitos no solamente con los anexos que establecen la evaluación de conformidad (IX y XI) sino también con el de requisitos generales de seguridad y funcionamiento anexo I y articulo 10 de requisitos. read more…
Memoria @AEMPSgob 2018 – primer año de Directora de Maria Jesús Lamas Diaz ( @chuslamas )
Cuando Mª Jesús Lamas cumple el primer año como Directora, la AEMPS publica la memoria de 2018 en la que se hace balance del año. Su primer año, aunque tomaba posesión del cargo el 1 de agosto frente a la entonces ministra Carmen Montón, por lo que entendemos que aun cerraba el año planificado por su predecesora. Lamas que representa un cambio generacional en la Dirección de la AEMPS contando con perfil en redes sociales como parte de su trabajo y con experiencia en el ámbito hospitalario no contaba con la visión industrial y suponemos que se ha visto sorprendida con en el cambio super relevante (cada veinte años) al que están sujetos los productos sanitarios, pasando de Directivas a Reglamentos, el informe «Implant files», Reglamentos de ensayos clínicos y mas horizontalmente con el BREXIT.
Con 116 páginas la memoria del 2018 aporta datos relativos al sector de productos sanitarios. Veamos algunos
Vigilancia: 6.294 notificaciones= 5.061 incidentes + 1.188 FSCA.
Tipo de productos afectados: implantes activos 13,6%, implantes no activos 36,8%, electromedicos 22,2%, IVD 9,5% y otros 18%
Como resultado del informe «implant files» que incluía muchas verdades a medias que cualquier persona del sector vería como falsos (como el «marcado CE» de las mallas de mandarinas) se tiene mayor transparencia en las alertas que se publican ahora en el portal de la AEMPS: https://sinaem4.aemps.es/alertas/alertasPublicadas.do
En cuanto al Organismo Notificado 0318:
446 PRODUCTOS CERTIFICADOS CE NUEVOS Y PRORROGADOS
40 CERTIFICADOS ISO 13485 NUEVOS Y PRORROGADOS
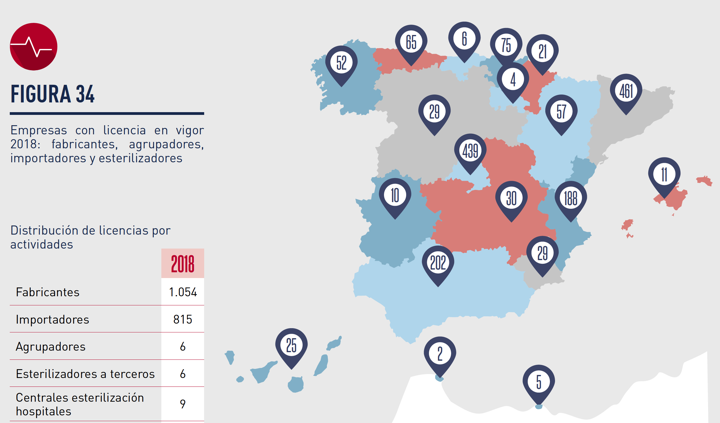
Las licencias de productos sanitarios se han incrementado el 2018 en 140 y se han dado de baja 192, es decir un crecimiento negativo. Esta figura es nos indica como estan repartidas las instalaciones de fabricación en España:
Nótese que tenemos una concentración de ellas en:
– 27% Cataluña
– 26% Madrid
– 12% Andalucia
– 11% Valencia
– 4% Pais Vasco
– 3% Cantabria
– 3% Aragon
– 3% Galicia
En el capitulo I de personal se indican 526 trabajadores en esta. No se indica cuantos técnicos trabajan en Productos Sanitarios pero teniendo en cuenta la preparación para los Reglamentos parecería lógico que este personal se hubiera incrementado para afrontar este reto y en cambio se da como causa del aumento el Brexit.
Esta memoria junto al plan estratégico para 2019-2022 establece los 5 objetivos estratégicos de la AEMPS para este periodo.
OBJETIVO ESTRATÉGICO 1: Garantizar a la ciudadanía la calidad, seguridad, eficacia, disponibilidad e información de los medicamentos y productos sanitarios, así como la calidad y seguridad de cosméticos y productos de cuidado personal
OBJETIVO ESTRATÉGICO 2: Incrementar la transparencia, y la accesibilidad y la satisfacción de los usuarios
OBJETIVO ESTRATÉGICO 3: Ser reconocida como referente nacional e internacional por los grupos de interés y promover la investigación
OBJETIVO ESTRATÉGICO 4: Mejorar la gestión económica y organizativa
OBJETIVO ESTRATÉGICO 5: Mejorar los recursos y las capacidades de la AEMPS mediante el desarrollo de las personas, la tecnología y las alianzas estratégicas
La Directora indica en su presentación: «En lo que respecta a la certificación de productos sanitarios, la AEMPS ha trabajado duramente a lo largo de 2018 para solicitar su designación como Organismo Notificado, en virtud del Reglamento 2017/745, de 5 de abril, sobre productos sanitarios.» aunque no sabemos bien en que plan de acción esta esta designación. Esperamos que la AEMPS se de cuenta de la gravedad del momento regulatorio y abran un plan de acción específico para los Reglamentos de Productos Sanitarios y no perdamos esta oportunidad de mejora asociada a este cambio.
Nuevas tasas de FDA para medical devices de FY2020 @FDAdeviceInfo
Tipo de registro TASA-FY2020** TASA-FY2020(SMALL BUSINESS*)
510k 11594$USA 2899$USA
de NOVO 102299$USA 25575$USA
Establishment 5236$USA 5236$USA (no hay descuento)
(Register&Listing)
PMA 340995$USA 85249$USA
*SMALL BUSINESS = Facturación 2019 < 100 millones $USA (certificado por la AET)
**Fiscal Year 2020 (FY2020) = 1/Octubre/2019 hasta 30/Septiembre/2020
Subida de ambas tasas mas relevantes de la FDA, la de 510k y la de registro (establishment)
Tecno-med realiza estos tramites y la asesoría en la documentación, para su empresa, solicítanos oferta