PRODUCTOS SANITARIOS


.
REGLAMENTO MDR (EU) 2017/745
MDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2021
RD 192/2023
RD – ingles
entrada en vigor: 23 marzo 2023
«legacy» s/reglamento 2023/607
IIb(implante) y III -31 dic 2027
IIa, IIb(no implant) y I (ON) -31 dic 2028
sin fin periodo distribución
.
PRODUCTOS SANITARIOS IVD


.
REGLAMENTO IVDR (EU) 2017/746
IVDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2022
RD IVD
entrada en vigor: 2024?
«legacy»s/reglamento 2024/1860
clase D – 31 Dic 2027
clase C – 31 Dic 2028
clases B y As – 31 Dic 2029
sin fin periodo distribución
.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
#COVID19 FAQ regulatorias (4) – La Comision Europea (@SKeersmaecker) propone el aplazamiento de 1 año en la fecha de aplicación del reglamento MDR

#COVID19 FAQ regulatorias (2) – Ventiladores pulmonares (o respiradores) y sus requisitos
Los ventiladores pulmonares (o respiradores) son equipos electromédicos para facilitar la respiración que usan presión para enviar aire, o una mezcla de gases, hacia los pulmones. Son cruciales para la atención de las personas con insuficiencia pulmonar, que puede ser una de las complicaciones que sufren los pacientes con casos graves de COVID19. Los ventiladores también se pueden configurar para exhalar aire, asumiendo efectivamente las funciones de inhalación y exhalación. Se programan para que «respiren» a un ritmo determinado de acuerdo con las necesidades del paciente. Ver en Medline información sobre estos equipos
Hay diversos tipos de equipos electromédicos usados en asistencia respiratoria, os ponemos las características del de cuidados críticos:
Ventiladores pulmonares de cuidados críticos (UCI)
norma EN ISO 80601-2-12 Requisitos particulares para la seguridad básica y el funcionamiento esencial de los ventiladores de cuidados críticos

#COVID19 FAQ regulatorias (1) – Mascarillas y requisitos
Tal y como aparece en la ilustración de @ AFP hay dos grandes tipos de mascaras de protección mas usadas:
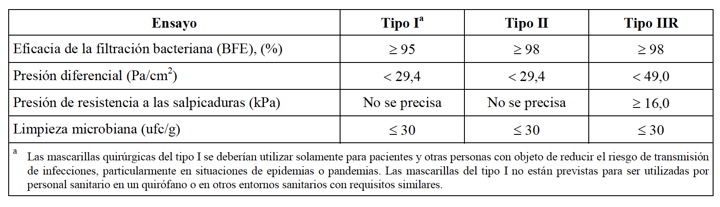
1. mascarillas quirúrgicas
norma EN 14683 Mascarillas quirúrgicas – Requisitos y métodos de ensayo
NO precisan de intervención de Organismo Notificado
Es una buena práctica también solicitar el certificado de ensayo según la norma EN 14683 con la eficacia del filtro.

MDCG: nuevas publicaciones MDCG 2020-3

MDCG: nuevas publicaciones MDCG 2020-2

MDCG: nuevas publicaciones MDCG 2020-1
![Guía IAF [ @IAF_Global ] para la realización de auditorias de calidad y reglamentarias en circunstancias extraordinarias (e.g. COVID19)](https://www.tecnologias-sanitarias.com/wp-content/uploads/2020/03/IAF-COVID19-1080x675.png)
Guía IAF [ @IAF_Global ] para la realización de auditorias de calidad y reglamentarias en circunstancias extraordinarias (e.g. COVID19)
La IAF (International Accreditation Forum) es la asociación mundial de organismos de acreditación de evaluación de la conformidad y otros organismos interesados en la evaluación de la conformidad en los campos de sistemas de gestión, productos, servicios, personal y otros programas similares de evaluación de la conformidad. Su función principal es desarrollar un único programa mundial de evaluación de la conformidad que reduzca el riesgo para las empresas y sus clientes al asegurarles que se puede confiar en los certificados acreditados. La acreditación asegura a los usuarios la competencia e imparcialidad del organismo acreditado. read more…
FAQ UDI -update ¿Cuando, donde, como ? EU – UDI según reglamentos MDR e IVDR
Como tenemos muchas consultas os actualizamos este tema …
Los plazos establecidos por el Reglamento de MDR para la inclusión del UDI en el etiquetado son
(no se aplica a los productos sanitarios a medida, ni a los destinados a investigación clínica / evaluación del funcionamiento, ni a los «legacy»)
parece pues que tenemos mucho tiempo para tratar el tema de UDI,
y además con el retraso anunciado de la puesta en marcha de EUDAMED a 26 de mayo de 2022 …
No obstante: La obligación de asignación de UDI se aplica a partir de la fecha de aplicación de los dos nuevos Reglamentos, es decir, el 26 de mayo de 2020 para productos sanitarios y el 26 de mayo de 2022 para productos sanitarios para diagnóstico in vitro.
La asignación de UDI se realiza por el fabricante en una de las Entidades designadas por la Comisión Europea, siendo la mas extendida la GS1 AISBL (AECOC en España). Es decir, que antes de 26 de mayo de 2020 debemos tener un código UDI con GS1-AECOC para todos nuestros productos
La obligación de presentar datos UDI en la base de datos de Eudamed se aplica obligatoriamente a partir del 26 de mayo de 2022 pero ya se ha anunciado que en mayo de 2020 podremos dar de alta los datos para evitar la acumulación de comunicaciones en 2022.
Ven a nuestra formación ONLINE sobre UDI:
Prohibición de la FDA @FDAcdrhindustry para los dispositivos de estimulación eléctrica (ESD) para conductas autolesivas o agresivas
Con fecha 6 de abril de 2020 quedan prohibidos los dispositivos de estimulación eléctrica ESD (ESD) para conductas autolesivas o agresivas en Estados Unidos. Esta prohibición incluye tanto dispositivos nuevos como dispositivos que ya están en distribución y uso.
Esta regla se aplica solo a los ESD utilizados para conductas autolesivas o agresivas y no se aplica a los dispositivos de acondicionamiento aversivo utilizados para otros fines, como los utilizados para dejar de fumar, que están fuera del alcance de esta regla, u otros aprobados por la FDA o dispositivos o tecnologías aprobados, como los estimuladores de electroterapia craneal o la estimulación magnética transcraneal, que tienen una garantía razonable de seguridad y efectividad para diferentes indicaciones.