PRODUCTOS SANITARIOS


.
REGLAMENTO MDR (EU) 2017/745
MDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2021
RD 192/2023
RD – ingles
entrada en vigor: 23 marzo 2023
«legacy» s/reglamento 2023/607
IIb(implante) y III -31 dic 2027
IIa, IIb(no implant) y I (ON) -31 dic 2028
sin fin periodo distribución
.
PRODUCTOS SANITARIOS IVD


.
REGLAMENTO IVDR (EU) 2017/746
IVDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2022
RD IVD
entrada en vigor: 2024?
«legacy»s/reglamento 2024/1860
clase D – 31 Dic 2027
clase C – 31 Dic 2028
clases B y As – 31 Dic 2029
sin fin periodo distribución
.
PROXIMA FORMACIÓN
Jornada formacion @Tecno_Sanitaria «P.SANITARIOS DE AUTO-CERTIFICACIÓN y LEGACY – CUMPLIMIENTO MDR»
Después de que se aprobara el Corrigendum 2 del Reglamento de MDR nos han quedado menos productos sanitarios en cuenta atrás pero no podemos bajar la guardia. read more…
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
#37SymposiumAEFI de @AEFI_es Barcelona 7 y 8 Junio – con la participación de @tecno_med
Como cada año no te pierdas este evento http://www.aefi2017.com de la AEFI (Asociación los Farmacéuticos de la Industria) este año toca en Barcelona.
El programa cuenta con numerosas ponencias sobre productos sanitarios con la presencia de las Autoridades Sanitarias tanto de la AEMPS como de Cataluña.
y no te pierdas nuestro taller
“Validación de software y procesos informatizados en la industria de los productos sanitarios” Claire Murphy
Somos empresa colaboradora en este Symposium:
Este es el programa para PRODUCTOS SANITARIOS:
Jueves, 8 de junio
09.00-10.30h Sala Auditorium
Mesa 12: Nuevos Reglamentos de Productos Sanitarios: últimas novedades y visión de la industria para afrontar el cambio.
Moderadora: Susana Andueza. Jefe de Servicio de Inspección de Farmacia Área de Sanidad. Delegación de Gobierno en Cataluña.
– Últimas novedades. Mª Carmen Abad. Jefe Departamento Productos Sanitarios AEMPS
– Visión de la industria para afrontar el cambio. María Aláez. Directora Técnica FENIN
11.00-12.30h Sala Liberty
Taller 5: Validación de software y procesos informatizados en la industria de los productos sanitarios
Moderadora: Mª Ángeles Bravo. Directora Técnica de PROCLINIC S.A.
– Claire M. Murphy.Socio Consultor Tecno-med Ingenieros
12.30 – 14.00h Sala Eiffel+ Sears+Pisa
Mesa 17: Norma ISO13485:2016
Moderadora: Mª Eugenia Villanueva. Vocal de Productos Sanitarios. AEFI– Sección Catalana
– Nuevos retos para los diferentes agentes económicos. Loreto del Rio Bermúdez. SGS Medical Devices- Health Services Manager
– Punto de vista de la industria. Caso práctico. Anna Mir. Directora Técnica DELTALAB
revisa el programa entero.
Sede: Hotel Hesperia Tower, Gran Via, 144 – 08907 Hospitalet de Llobregat Barcelona (España) Tel. +34 93 4135000
5 abril 2017 – Aprobado por el Parlamento Europeo el Reglamento de Productos Sanitarios para diagnóstico in vitro (IVDR)

Tal y como ya os habiamos anunciado el Parlamento Europeo ha aprobado el Reglamento de Productos Sanitarios. Ahora solo falta su publicación en el DOUE y entrará en vigor a los 20 días de su publicación (fecha de entrada en vigor prevista junio 2017) y su fecha de aplicación según el periodo transitorio de 5 años, que se indica en su articulo 113, será el año 2022.
Ver la nota de prensa de la Comisión Europea: http://europa.eu/rapid/press-release_IP-17-847_es.htm
Os dejamos aqui una copia en español para vuestra información:
https://www.dropbox.com/s/kfz8esndy79ir6o/IVDR-PE_15_2017_INIT_ES.pdf?dl=0
Estamos preparando unas jornadas de formación que pensamos pueden ser de tu interés:
Barcelona 6 de Julio de 2017 IVDR![]()
Madrid 13 de Julio de 2017 IVDR![]()
Esperamos contar con tu presencia. Gracias por tu confianza read more…
Congreso AIIC Asociación Italiana de Ingenieria Clínica 6-8 abril Genova en la que participa la SEEIC
La sociedad hermana de la SEEIC (Sociedad Española de Electromedicina e Ingenieria Clinica) española celebra el Congreso nacional de la AIIC (Asociación Italiana de Ingenieria Clínica) los próximos 6 a 8 de abril en Genova. Visita su web: http://www.convegnonazionaleaiic.it/
En la mesa redonda “La introducción de la innovación en los diversos países: El punto de vista de los ingenieros clínicos europeos” colabora la SEEIC presentando la visión española su vicepresidente Xavier Canals
HEALTHIO 3 a 5 mayo 2017 Barcelona
Healthio es un evento novedoso, dinámico e interactivo que cuenta con actividades organizadas por áreas específicas para la innovación en el sector de la salud.
Es un evento interactivo con actividades sobre la innovación en sanidad. Cuenta con participantes de todos los ámbitos y perfiles sanitarios.
Como podeis ver es una iniciativa mas, conjunta entre diversos actores para atraer materia gris a los congresos de Barcelona, no todo van a ser eventos de ventas …
Inscribete: http://www.healthio-global.com/choose-your-role
Congreso CEDEST 5-7 abril 2017 Alicante
Como cada años la asociación de los expertos de esterilización españoles CEDEST se reúne en Alicante. Hoy 5, arranca con el simposium satélite y mañana es la inauguración. read more…
Congreso AIIC Asociación Italiana de Ingenieria Clínica 6-8 abril Genova en la que participa la SEEIC
La sociedad hermana de la SEEIC (Sociedad Española de Electromedicina e Ingenieria Clinica) española celebra el Congreso nacional de la AIIC (Asociación Italiana de Ingenieria Clínica) los próximos 6 a 8 de abril en Genova. Visita su web: http://www.convegnonazionaleaiic.it/
En la mesa redonda “La introducción de la innovación en los diversos países: El punto de vista de los ingenieros clínicos europeos” colabora la SEEIC presentando la visión española su vicepresidente Xavier Canals read more…
Congreso EUREC-ANCEI Asociaciones Europeas de Comités Eticos de Investigación Clínica 17-19 Mayo en Barcelona
Congreso Conjunto EUREC-ANCEI(European Network of Research Ethics Committees – Asociación Nacional de Comités de Ética de la Investigación) que tendrá lugar los días 17-19, 2017 de Mayo en Barcelona con el lema : “El Futuro de los Comités Éticos de Investigación en Europa: Creando el camino hacia la Innovación”. Visita la web del congreso: https://eurec-anceicongresbarcelona2017.org/ en este participa Tecno-med en una mesa redonda. read more…
Jornada “Forum de talento en Ingenieria Biomedica” 2 Marzo 2017

Interesante jornada organizada por las tres universidades de Barcelona que dan el grado de ingeniería biomédica conjuntamente con las organizaciones FENIN y HeathTech Cluster el 2 de marzo en el paraninfo de la Facultad de Medicina de la UB. read more…
@FARMAFORUM foro industria farma – ven a nuestra conferencia de evaluación clínica de productos sanitarios 2 Marzo 2017 15h30
Infors@lud 2017 Congreso Nacional de Informática de la Salud, Madrid 21-23 Marzo
La sanidad no es ajena a las transformaciones que las nuevas tecnologías producen en la industria, modelos de negocio y mercados y vemos como las estrategias en la utilización de las Tecnologías de la Información y Comunicación (TIC) tiene un papel fundamental a la hora de afrontar la necesaria transformación de los sistemas de salud. Para la XX edición, el Congreso de INFORSALUD 2017 ha elegido como lema La transformación digital del sector de la salud. read more…
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
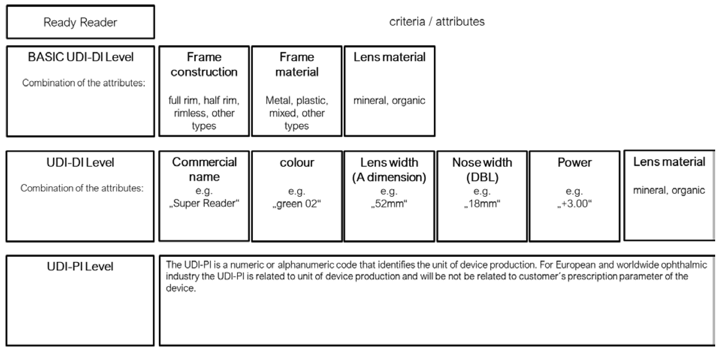
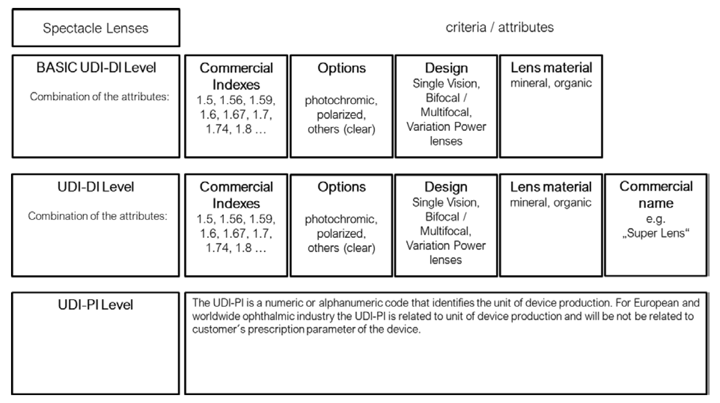
MDCG: nueva MDCG 2020-18 para el UDI de las lentes ópticas y gafas premontadas
Publicada la MDCG 2020-18 «Posittion paper on UDI assignement for spectacle lentes and ready readers» que indica como establecer el UDI a estos productos precediendo al de lentes de contacto que también tendrá una MDCG especial asociada al UDI
FELICES FIESTAS !!!
Loreto del Río Medical Devices Manager de @SGS hace entrega a Tecno-med Ingenieros @tecno_med del certificado ISO 13485
El alcance del certificado emitido por la entidad de certificación SGS es:
«Servicios de consultoría en aspectos clínicos y regulatorios, implantación y mantenimiento de sistemas de gestión de la calidad, formación y servicios relacionados aplicables a la industria de productos sanitarios»
Muchas gracias a todos
Tecno-med Ingenieros @tecno_med primera Consultoria española que obtiene el certificado ISO 13485
El alcance del certificado emitido por la entidad de certificación SGS es:
«Servicios de consultoría en aspectos clínicos y regulatorios, implantación y mantenimiento de sistemas de gestión de la calidad, formación y servicios relacionados aplicables a la industria de productos sanitarios»
Muchas gracias a todos
MDCG: nueva MDCG 2020-17 con las FAQ sobre auditorias remotas de los ON
Publicada la revisión de la guia MDCG 2020-4 «Guidance on temporary extraordinary measures related to medical device notified body audits during COVID-19 quarantine orders and travel restrictions» mediante un FAQ de esta guía. Nos da algunas pautas como que por ejemplo esta auditoria remota debe incluir una visita a a las instalaciones y entrevistas con trabajadores. Si deja la aplicación de estas a estudiar y justificar caso a caso.
Como siempre nos resuelve algunas dudas y nos abre otras …
![]()
El próximo 1 de diciembre se abre el modulo de registro de actores de EUDAMED
Se publican ademas las FAQ sobre EUDAMED:
https://ec.europa.eu/health/md_eudamed/actors_registration_en
Aunque como ya todos sabéis la fecha de puesta en marcha de EUDAMED es 22 de mayo de 2022 la Comisión Europea ha confirmado su interés en hacer disponibles los 6 módulos gradualmente, y ha anunciado la apertura del modulo de registro de actores incluyendo el uso del SRN (Single Registration Number) el 1 de Diciembre de 2020 animando a todos los actores al uso de este modulo incluyendo los SRN en los certificados y a evitando, en la medida de lo posible, dobles registros para los actores.
Publicado RD 957/2020 «Estudios observacionales con medicamentos»
En este RD se incluyen modificaciones también relativas al Estatuto de la Agencia Española de Medicamentos y Productos Sanitarios incluido en el Real Decreto 1275/2011. Estas modificaciones afectan al Comité de Productos Sanitarios y se crea el Comité Técnico del Área de Certificación incluyendo en este último a un miembro experto de FENIN.
Entrará en vigor el próximo 2 de Enero de 2021.
La @AEMPSgob publica una nota informativa sobre los test COVID
La SEEIC abre la iniciativa #SEEIC_training en su portal de formación
El primer #SEEIC_training lo imparte Paloma Longarela de GE Healthcare. Inscríbete gratuitamente en la pagina web de la SEEIC para formación: https://training.seeic.org