PRODUCTOS SANITARIOS


.
REGLAMENTO MDR (EU) 2017/745
MDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2021
RD 192/2023
RD – ingles
entrada en vigor: 23 marzo 2023
«legacy» s/reglamento 2023/607
IIb(implante) y III -31 dic 2027
IIa, IIb(no implant) y I (ON) -31 dic 2028
sin fin periodo distribución
.
PRODUCTOS SANITARIOS IVD


.
REGLAMENTO IVDR (EU) 2017/746
IVDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2022
RD IVD
entrada en vigor: 2024?
«legacy»s/reglamento 2024/1860
clase D – 31 Dic 2027
clase C – 31 Dic 2028
clases B y As – 31 Dic 2029
sin fin periodo distribución
.
PROXIMA FORMACIÓN
Formación «2102 – Gestión de Riesgos según MDR/IVDR y EN ISO 14971» 16 Marzo 2021 9h-14h
Fecha: 16 Marzo 2021, 9h a 14h en webinar en directo y 25h en teleformacion
La gestión de riesgos es una herramienta fundamental en el diseño y la fabricación de los productos sanitarios siendo de aplicación la norma EN ISO 14971:2019. Además, los nuevos reglamentos MDR e IVDR nos obligan a mantener un sistema que contemple todo el ciclo de vida (incluyendo subcontratistas) y la revisión continua de los riesgos en base al PMS y PMC(P)F. En esta formación, conoceremos los detalles de la aplicación de estas normas con los nuevos reglamentos.
![]()
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
XXV Congreso de Derecho Sanitario @aeds_es 18-20 Oct’2018. Mesa “Nuevos reglamentos europeos de productos sanitarios” by @FENIN_es
Moderado por Margarita Alfonsel Secretaria General de FENIN y con la participación de los expertos: Maria Alaez, Directora Técnica de FENIN, Mª Carmen Abad Jefa Departamento Productos Sanitarios de la AEMPS y Jesus Rueda Director de International Affairs de MEDTECH. read more…
Congreso ORTO Medical Care 25-26 Oct’ 2018 Madrid by @FEDOP20

La feria ortoprotésica OMC está dirigida a profesionales del sector de la ortoprotésica, ayudas técnicas, movilidad y productos destinados al cuidado de la tercera edad, en IFEMA del 25 al 26 de Octubre de 2018. read more…
Reunión del CTN209/SC62 “Equipos eléctricos en la practica médica” de @normasUNE
Se celebró la reunión del subcomité de UNE que participa en la elaboración de la normativa internacional y española de electromedicina para revisar las distintas normas en proceso de aprobación. Como siempre Jose Antonio Jimenez jjimenez@une.org estuvo al frente de la reunión moderando las distintas aportaciones. read more…
Día Mundial de la Normalización 14’Oct 2018 “Normas internacionales y la 4 Revolución Industrial” @AENOR @NormasUNE @IECstandards @ISOstandards @ITU
Este año, el Día Mundial de la Normalización tiene como lema “Normas internacionales y la 4 Revolución Industrial”. Con él, los organismos de normalización internacionales —la Organización Internacional de Normalización (ISO), la Comisión Electrotécnica Internacional (IEC) y la Unión Internacional de Telecomunicaciones (ITU) — han querido destacar como las normas que fueron cruciales en la 1ª revolución industrial, hace 250 años, también lo serán en la 4ª.
HEALTHIO 16 a 18 octubre 2018 @healthioglobal organizado por @Fira_Barcelona
En su segunda edición y dentro de la Barcelona Industry Week que une tres grandes eventos para hacer frente a la 4a Revolución Industrial: HEALTHIO, IN(3D)USTRY From Needs to Solutions e IOT Solutions World Congress presenta una agenda amplia y transversal que según los organizadores permitirá al visitante descubrir todos los avances y novedades del ámbito sanitario.
MEDICON 2019 – 26 a 28 Septiembre en Portugal inicia su convocatoria @2919Medicon
Exito formación “Evaluación clínica de Productos Sanitarios según MDR” by @SGS_Spain 1-2 Oct 2018 9h a 18h Madrid
Exito Jornada SEEIC 28 Sept 2018 Madrid “La seguridad en la Electromedicina e Ing Clínica: un compromiso compartido” con la participación de @XCanals

28 septiembre 2018 Clínica Universidad de Navarra Calle Marquesado de Sta. Marta, 1, 28027 Madrid
Con un centenar de asistentes se celebró el pasado viernes 28 de septiembre la Jornada SEEIC “La seguridad en la Electromedicina e Ingeniería Clínica: un compromiso compartido”. En ella pudimos ver el gran interés que se generó sobre las distintas ponencias debido al enfoque “hands on” de las mesas de la SEEIC.
Formación “Evaluación clínica de Productos Sanitarios según MDR” by @SGS_Spain 1-2 Oct 2018 9h a 18h Madrid
Premios Tecnología y Salud 2019 – 2 Oct 19h Madrid con @FENIN_es
No te pierdas este evento … próximo 2 de octubre a las 18:30 horas Entrega de los Premios “Tecnología y Salud 2019, que será presidido por María Luisa Carcedo Roces, Ministra de Sanidad, Consumo y Bienestar Social,
que tendrá lugar en:
Edificio Nouvel / Auditorio 400 – Museo Reina Sofía
Calle Santa Isabel, 52, • 28012 Madrid
y en el que se hará entrega del:
- XI Premio Fenin a la Innovación Tecnológica Sanitaria 2019.
- Reconocimiento de la Fundación Tecnología y Salud 2019.
- Premio de la Fundación Tecnología y Salud a la mejor organización de apoyo al paciente 2019.
- Premio de la Fundación Tecnología y Salud al mejor programa de Crónicos impulsado por una CC.AA 2019.
- Premio de la Fundación Tecnología y Salud al mejor programa de Educación y Prevención en Salud promovido por una CC.AA 2019.
- Premio de la Fundación Tecnología y Salud a la mejor Innovación Tecnológica en Salud impulsada por una CC.AA. 2019.
- Premio Fenin al Emprendimiento en Tecnología Sanitaria 2019.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.

Publicado Real Decreto 588/2021 para regular la venta al publico y publicidad de ps IVD autodiagnostico para COVID-19
Hoy el BOE publica el Real Decreto 588/2021 modificando la venta y publicidad con productos sanitarios para IVD de autodiagnóstico en España análogamente a como han hecho otras autoridades sanitarias como las alemanas.
A destacar:
– se aplica sólo a las pruebas de IVD de autodiagóstico (antígenos y anticuerpos) que precisan pues de intervención de Organismo Notificado (llevan número de ON con el símbolo CE)
– se podrán vender en farmacia sin receta médica los test de autodiagnóstico para COVID-19 (no es necesaria prescripción)
– se puede efectuar publicidad dirigida al publico de productos de autodiagnostico para COVID-19, aunque como siempre es preceptiva la autorización de esta por parte de las autoridades sanitarias de la CCAA.
– entra en vigor el 21 de julio de 2021![]()

Publicada la primera lista de normas armonizadas con MDR – Decisión de Ejecución 2021/1182
Tal y como indica en el texto de la Decisión de Ejecución 2021/1182 : «La conformidad con una norma armonizada confiere la presunción de conformidad con los requisitos esenciales correspondientes establecidos en la legislación de armonización de la Unión a partir de la fecha de publicación de la referencia de dicha norma en el Diario Oficial de la Unión Europea» y la fecha de publicación en el DOUE es 19 julio 2021
La lista es cortita:
N. Referencia de la norma
1. EN ISO 10993-23:2021 Evaluación biológica de productos sanitarios. Parte 23: Ensayos de irritación (ISO 10993-23:2021)
2. EN ISO 11135:2014 Esterilización de productos sanitarios. Óxido de etileno. Requisitos para el desarrollo, la validación y el control de rutina de un proceso de esterilización para productos sanitarios (ISO 11135:2014) EN ISO 11135:2014/A1:2019
3. EN ISO 11137-1:2015 Esterilización de productos para asistencia sanitaria. Radiación. Parte 1: Requisitos para el desarrollo, la validación y el control de rutina de un proceso de esterilización para productos sanitarios (ISO 11137-1:2006, incluida la modificación 1:2013) EN ISO 11137-1:2015/A2:2019
4. EN ISO 11737-2:2020 Esterilización de productos para la salud. Métodos microbiológicos. Parte 2: Ensayos de esterilidad efectuados para la definición, validación y mantenimiento de un proceso de esterilización (ISO 11737-2:2019)
5. EN ISO 25424:2019 Esterilización de productos para la salud. Vapor de agua y formaldehído a baja temperatura. Requisitos para el desarrollo, validación y control de rutina de un proceso de esterilización para productos sanitarios (ISO 25424:2018)
![]()

MDCG: avalancha de guías MDCG antes de coger vacaciones …
Los distintos grupos de trabajo finalizan diversas guías (se nos acumula la lectura):
MDCG 2021-13 rev.1 – «Questions and answers on obligations and related rules for the registration in EUDAMED of actors other than manufacturers, authorised representatives and importers subject to the obligations of Article 31 MDR and Article 28 IVDR» – July 2021 ![]()
MDCG 2021-14 – «Explanatory note on IVDR codes» – July 2021 ![]()
MDCG 2021-15 – «Application form to be submitted by a conformity assessment body when applying for designation as notified body under Regulation (EU) 2017/745 on medical devices (MDR)» – July 2021 ![]()
MDCG 2021-16 – «Application form to be submitted by a conformity assessment body when applying for designation as notified body under Regulation (EU) 2017/746 on in vitro diagnostic medical devices (IVDR)» – July 2021 ![]()
MDCG 2021-17 – «Applied for scope of designation and notification of a conformity assessment body – Regulation (EU) 2017/745 (MDR)» – July 2021 ![]()
MDCG 2021-18 – «Applied for scope of designation and notification of a conformity assessment body – Regulation (EU) 2017/746 (IVDR)» – July 2021 ![]()
MDCG 2021-19 – «Guidance note integration of the UDI within an organisation’s quality management system» – July 2021 ![]()

@FENIN_es publica el informe «Estudio sobre la fabricacion de tecnologia sanitaria en España»
Nos encanta este informe de FENIN sobre los fabricantes españoles, lectura para finde y que esperemos llegue. Se destaca la necesidad de fortalecer este importante tejido productivo para disminuir la alta dependencia del exterior y dar respuesta con solvencia a eventuales emergencias sanitarias como las actuales.
La apuesta de los emprendedores y empresarios debe ser apoyada por las Administraciones Públicas para posibilitar su crecimiento y la internacionalización de las empresas del sector. Esto pasa por reforzar el ON español y la incentivación de la cultura de la calidad en el sector. En el informe se destaca que sigue siendo mayoritario el sector de productos sanitarios de un sólo uso y lo poco desarrollados que esta aun sectores como el de Salud Digital. Encontramos a faltar la valoración del impacto de los nuevos reglamentos en el sector …


Nuevo borrador de la BS/AAMI 34971 Guia de aplicación de la ISO 14971 de gestión de riesgos a la Inteligencia artificial

Boletin @AEMPSgob 2T 2021 de productos sanitarios y cosméticos

Publicada la nueva edición de la norma de símbolos ISO 15223-1:2021

Por fin se publica la ISO 15223-1:2021 de símbolos utilizados en los productos sanitarios que incluye símbolos requerido por los reglamentos como el de producto sanitario MD, el de los agentes económicos y el de las actividades que puede realizar un distribuidor como reenvasado y traducción de instrucciones de uso.
La puedes adquirir en ISO https://www.iso.org/standard/77326.html
y pronto la podrás adquirir la versión en español en UNE https://www.une.org/encuentra-tu-norma/busca-tu-norma
Las novedades que indica la propia norma en su introducción son:
– adición de 20 símbolos que fueron validados según ISO 15223-2;
– adición de 5 símbolos previamente publicados en ISO 7000, ISO 7001 e IEC 60417;
– supresión de la definición de «etiquetado» (labelling);
– inclusión de terminología utilizada en ISO 20417, ISO 13485 e ISO 14971;
– ampliación de los ejemplos que figuran en el anexo A;
– la información sobre los reglamentos europeos se ha trasladado siempre a notas informativas.


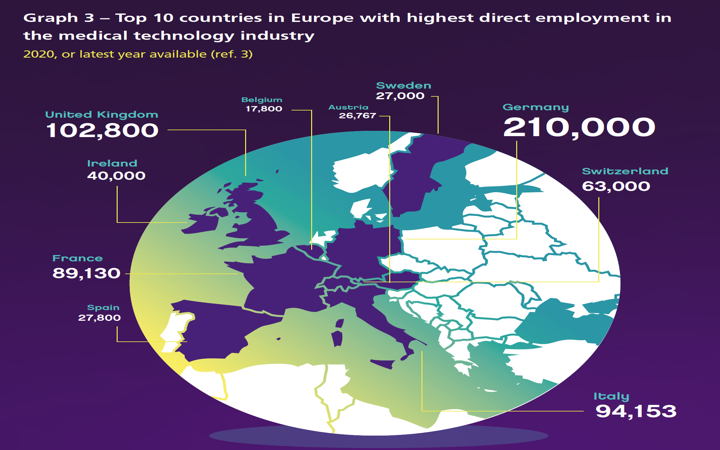
@MedtechEurope ( @FENIN_es ) publica el informe «The European Medical Technology Industry in figures 2021»
En este informe se destaca el alto nivel de empleo de este sector que incluye mas de 500.000 tipos de productos y que emplea directamente mas de 760.000 personas en Europa frente por ejemplo a los 795.000 que emplea el sector farmacéutico, siendo aproximadamente un 0.3% del empleo total en Europa. Entre los 10 primeros países con mayor empleo directo del sector de tecnologías sanitarias se encuentra España.

Nueva guia PICS sobre ‘Good practices for DATA MANAGEMENT and INTEGRITY in regulated GMP/GDP environments’
La PICS ha publicado la guía para aclarar el tratamiento de de los Sistemas de Gestión de la Calidad gestionados por aplicaciones informáticas, identificando los riesgos en estos sistemas informatizados. Como siempre útil también para su aplicación a los sistemas de gestión de calidad de tecnologías sanitarias.