PRODUCTOS SANITARIOS


.
REGLAMENTO MDR (EU) 2017/745
MDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2021
RD 192/2023
RD – ingles
entrada en vigor: 23 marzo 2023
«legacy» s/reglamento 2023/607
IIb(implante) y III -31 dic 2027
IIa, IIb(no implant) y I (ON) -31 dic 2028
sin fin periodo distribución
.
PRODUCTOS SANITARIOS IVD


.
REGLAMENTO IVDR (EU) 2017/746
IVDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2022
RD IVD
entrada en vigor: 2024?
«legacy»s/reglamento 2024/1860
clase D – 31 Dic 2027
clase C – 31 Dic 2028
clases B y As – 31 Dic 2029
sin fin periodo distribución
.
PROXIMA FORMACIÓN

Formación «2204T – Reglamento IVDR y RD IVD en la de fecha aplicación IVDR» – grabación 26 Mayo 2022
Grabado en fecha: 26 Mayo 2022, 5h de grabación de directo y 25h en teleformación
Inscribete en esta formación y conoce los detalles de última hora de la aplicación del IVDR y la estrategia de operación para los distintos actores
PROGRAMA
1. Introducción. Estado
2. Fabricantes
3. Importador y EC-REP
4. Distribuidor
5. Usuarios (centros sanitarios, laboratorios clínicos, farmacias, médicos, pacientes,…)
6. Recomendaciones finales y coloquio.
![]()
El Reglamento (UE) 2017/746 (IVDR) que tiene como fecha de aplicación el próximo 26 de mayo de 2022 se complementa con el nuevo Real Decreto de productos sanitarios derogando en esta fecha la directiva 98/79/EC.
En este día tan relevante hicemos esta jornada donde abordamos el cambio de un modo práctico haciendo un resumen ejecutivo de estos y revisando que se espera de cada uno de nosotros según el rol que realizamos.
Revisamos los requisitos mas relevantes para los fabricantes, los importadores, los distribuidores, los representantes autorizados y los hospitales – laboratorios clínicos.
Veremos así las posibles estrategias y oportunidades de mercado de todos los agentes económicos y de los usuarios que van a ser los beneficiarios del cambio y esta adaptación al cambio la queremos sintetizar para vosotros con la filosofía del best-seller de S.Johnson “Quién se ha llevado mi queso”.
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.

Organismos Notificados: UDEM Adriatic d.o.o. (Croacia) ON num. 2696 nuevo ON (ya 18) con MDR. Enhorabuena!!!
Nueva designación del Organismo Notificado croata UDEM – Enhorabuena !!

puedes ver la lista de todos aqui en la base de datos NANDO:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34
y para IVDR … read more…
#COVID19 FAQ regulatorias – Kit autodiagnóstico IVD ya en farmacias
Test rápido anticuerpos COVID19 autodiagnóstico con marcado CE con intervención de Organismo Notificado
Se venden solo en farmacia y con receta. Son productos sanitarios para diagnóstico in vitro de uso por el propio paciente (no por profesionales) bajo el RD 1662/2000 – Dir 98/79, son productos de la clase otros (no pertenecen a la lista A o B de anexo II) pero son destinados a uso por el paciente (Producto para autodiagnóstico: Cualquier producto destinado por el fabricante para poder ser utilizado por profanos a domicilio).
Como cada año nosotros jugamos al 13485 en la lotería de Navidad !!
En producción el modulo de registro de actores de EUDAMED @EU_Health y registrados los primeros actores españoles validados por la @AEMPSgob
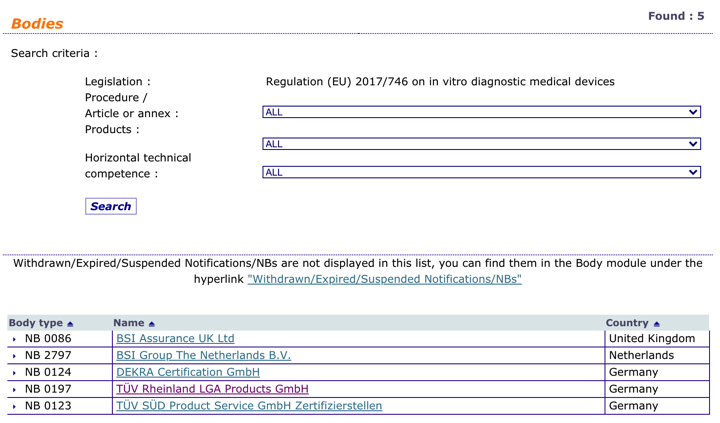
Organismos Notificados: TÜV Rheinland LGA Products ( @tuv_es ) NB num. 0197 nuevo ON con IVDR. Enhorabuena!!!
Nueva designación del Organismo Notificado alemán 0197 para IVDR
Enhorabuena !!
TÜV Rheinland LGA Products GmbH
Tillystraße 2, 90431 Nürnberg, Germany
Website : www.tuv.com/safety
Notified Body number : 0197
Este es su lista de códigos en el alcance de su notificación
Jornada Horizonte Europa 2021-27 para proyectos innovadores by @CDTIoficial
Nueva guía FDA @FDAcdrhindustry para EMC compatibilidad electromagnética de equipos electromedicos
Dia Mundial de la Calidad – 11 Nov 2020 by @AEC_es
Jornada interesante donde puedes ver que nos espera en la aplicación de las normas de calidad, no vemos a nadie de Sanidad … Lástima
A ver si hay suerte con alguno de los premios.
Programa
09:30 Recepción de Congresistas / Acceso virtual
09:30-09:40 Presentación Teresa Viejo
09:40-10:00 Bienvenida institucional Miguel Udaondo, Presidente, AEC y Raül Blanco, Secretario General de la Industria y de la Pyme
10:00-10:30 Conferencia inspiracional – Juan Verde, Líder global en desarrollo sostenible que ha trabajado con algunas de las personalidades más importantes del mundo como Barack Obama, Bill Clinton y Al Gore.
10:30-10:50 Entrega de Premio Líder en Calidad 2020 y Socio Distinguido AEC
1ª Entrega del Premio Líder en Calidad 2020
2ª Entrega de Socio Distinguido
10:50-11:40 Mesa redonda – Sesión Personas: AENOR, BANCO DE SANTANDER, CALIDAD PASCUAL, TAISI, nos inspirarán con sus Mejores Experiencias en Desarrollo Sostenible
Javier Mejía Martí, Director de Marketing Estratégico y de Producto, AENOR
Marta Aisa Blanco, Directora de Banca Responsable, BANCO SANTANDER
Joseba Arano Echebarría, Director de Gestión Ética, Responsable y Excelente, CALIDAD PASCUAL
Ruth Lázaro Torres, Directora General, TAISI
11:40-12:30 Mesa redonda – Sesión Planeta: ALSA, ENAGAS, FERROVIAL, TENDAM, nos inspirarán con sus Mejores Experiencias en Desarrollo Sostenible
Ignacio Pérez-Carasa González-Estrada, Director de Relaciones Institucionales, ALSA Grupo
José Miguel Tudela Olivares, Director de Organización y Sostenibilidad , ENAGAS
Ana Peña Laseca, Gerente de Calidad, Cambio Climático y Medio Ambiente FERROVIAL
Ana Fombella Posada, Directora de Comunicación y Responsabilidad Corporativa, TENDAM
12:30-13:00 Sostenibilidad es Calidad. Entrevista / diálogo. Avelino Brito, Director General, AEC
13:00-13:20 Premio Liderazgo Directivo
13:20-13:30 Cierre institucional Miguel Udaondo, Presidente, AEC

@RAPSorg «RAPS 2020 Euro Convergence» 26-30 Oct 2020 Bruselas
Esta semana estamos en la formación de RAPS https://www.raps.org/europe-2020/home , para ponernos al día con los grandes expertos europeos
Exito del webinar: «REGLAMENTO 2017/745 SOBRE LOS PRODUCTOS SANITARIOS. Puesta al día de los principales cambios que introduce el Reglamento 2017/745 sobre los Productos Sanitarios» by Maria Alaez @FENIN_es
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.

Organismos Notificados IVDR (7): 3EC (Eslovaquia) ON num. 2265 nuevo ON. Enhorabuena !!!
Nuevo Organismo Notificado para IVDR núm. 2265:
3EC International a.s.
Hranicna 18
Bratislava 82105 SLOVAKIA
Email : info@3ec.sk
Website : www.3ec.sk
puedes ver la lista siempre actualizada en la base de datos NANDO:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=35
y para MDR … read more…

La AEMPS modifica su estructura incluyendo el CNCPS como ON0318 para adaptarse a los reglamentos mediante el Real Decreto 271/2022 – @AEMPS_gob
Este RD establece el nuevo CNCPS modificando su estatuto del RD 1275/2011:
«3. Se adscribe a la Agencia Española de Medicamentos y Productos Sanitarios el Centro Nacional de Certificación de Productos Sanitarios como unidad con nivel orgánico de Subdirección General. Sin perjuicio de las especialidades recogidas en este Estatuto, se estará a lo dispuesto en el artículo 95.2 de la Ley 40/2015, de 1 de octubre, para la determinación de los servicios comunes.»
…
«Artículo 35 bis. El Centro Nacional de Certificación de Productos Sanitarios.
1. Al Centro Nacional de Certificación de Productos Sanitarios le corresponderá el ejercicio de las siguientes funciones:
a) Actuar como Organismo Notificado, evaluando la conformidad de los productos sanitarios y realizando las auditorias de los sistemas de calidad de los fabricantes, proveedores y/o subcontratistas que sean necesarias.
b) Certificar las normas de los sistemas de calidad y otras normas específicas del sector de productos sanitarios.
c) Emitir, modificar, restringir, suspender, renovar y revocar los certificados CE con vistas a la colocación del marcado CE en los productos sanitarios, en los términos que establezca la designación efectuada por el Ministerio de Sanidad.
d) Emitir, modificar, restringir, suspender, renovar y revocar los certificados de sistemas de calidad y otras normas específicas del sector de productos sanitarios.
e) Autorizar las entidades colaboradoras en la certificación de productos sanitarios.

MDCG: nueva MDCG 2022-5 Guía de productos sanitarios frontera con medicamentos – por fin tenemos la definición de mecanismos farmacológicos, inmunológicos y metabólicos
La @AEMPSgob amplia el registro de CCPS a productos sanitarios IVD según reglamento
Hasta que EUDAMED sea plenamente operativa, todos los productos en cuya certificación haya intervenido un organismo notificado (es decir, productos de la clase B, clase C y clase D) que se comercialicen en España, deberán realizar la comunicación de comercialización y/o puesta en servicio a través de la aplicación telemática CCPS, de acuerdo a lo establecido en el artículo 10 del Real Decreto 1662/2000. Para facilitar las comunicaciones se puede incluir en una misma comunicación aquellos productos que, perteneciendo a la misma clase, correspondan a la misma nomenclatura EMDN hasta mínimo el 4º nivel (W XX XX XX), e incluyendo todos los productos en el apartado de modelos.
Aqui encontraras la nota completa ![]()

Novedades MDSAP – Nueva edición de la guía de realización de auditorias ver.7 2022-04

La OMS @OMS_Spain publica las «Directrices para la vigilancia poscomercialización y la vigilancia del mercado de los productos sanitarios incluidos los de IVD»

ANVISA actualiza las GMP de productos sanitarios
ANVISA ha publicado el RDC 665/2022 que reemplaza a la version previa RDC 16/2013 y entra en efecto en 2 de Mayo de 2022. Ver texto

EUDAMED publica la guía de usuario de Operadores Economicos
Publicado «Indice SEIS» by @SEISeSalud con los datos de inversión en TIC de Salud en España
Publicado el informe ‘Índice SEIS’, estudio que elabora anualmente la SEIS, Sociedad Española de Informática de la Salud, y que detalla la inversión realizada en materia TIC por los centros sanitarios y consejerías de sanidad de España. El documento refleja un nuevo incremento en la inversión TIC por parte de la sanidad española en su conjunto (comunidades autónomas, Ministerio de Sanidad y Red.es) en 2021 hasta un 16,62%, llegando a 938 millones de euros. Sigue la tendencia de crecimiento de la telemedicina aunque no parece que estemos aprovechando la oportunidad de la pandemia para llevar esta a los niveles europeos. Puedes consultar el informe aqui