PRODUCTOS SANITARIOS


.
REGLAMENTO MDR (EU) 2017/745
MDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2021
RD 192/2023
RD – ingles
entrada en vigor: 23 marzo 2023
«legacy» s/reglamento 2023/607
IIb(implante) y III -31 dic 2027
IIa, IIb(no implant) y I (ON) -31 dic 2028
sin fin periodo distribución
.
PRODUCTOS SANITARIOS IVD


.
REGLAMENTO IVDR (EU) 2017/746
IVDR – ingles
entrada en vigor: 26 mayo 2017
fecha aplicación: 26 mayo 2022
RD IVD
entrada en vigor: 2024?
«legacy»s/reglamento 2024/1860
clase D – 31 Dic 2027
clase C – 31 Dic 2028
clases B y As – 31 Dic 2029
sin fin periodo distribución
.
PROXIMA FORMACIÓN

Formación «2205T – Gestión de Riesgos según Reglamentos MDR/IVDR y EN ISO 14971:2019+A11:2021» – grabación 28 Junio 2022 9h-14h
realizada en fecha: 28 Junio 2022, 9h a 14h en webinar en directo y 25h en teleformación.
Formación para conocer los detalles de última hora de la aplicación de la ultima edición de la norma armonizada de gestión de riesgos EN ISO14971:2012+A11:2021 y su aplicación práctica a los fabricantes de MDR / IVDR.
read more…
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
Foro de Inversión Healthcare Barcelona 24 Marzo 2021 by @COMBarcelona @Biocat_cat @BarcelonaActiva @ESADE con la participación de @tecno_med
El Foro de Inversión Healthcare Barcelona es un punto de encuentro entre emprendedores e inversores del sector sanitario. Se pueden presentar todo tipo de empresas con proyectos de Biotecnología, productos sanitarios, Servicios sanitarios y Tecnologías de la Información relacionadas con la salud. El Foro de Inversión Healthcare Barcelona se ha posicionado como referente en el ecosistema biomédico, promoviendo la innovación y el emprendimiento entre el colectivo con el objetivo de acercar emprendedores e inversores del sector sanitario participando en el mismo los actores principales motores de innovación de Barcelona. ![]()
Symposium AEFI 10-11 Mayo 2021 by @AEFI_es con la participación de @Tecno_med
Como cada año tenemos una cita en el SYMPOSIUM AEFI, este año del 10 al 11 de Mayo de 2021, con la participación de Tecno-med en
TALLER 3 «Clasificando Productos Sanitarios para Diagnóstico in Vitro» – 10 mayo 13h45 a 15h15 y
TALLER 9 “Reglamentos MDR/IVDR: Novedades en la información proporcionada con el producto» 11 mayo 15h a 16h
Ponentes: Xavier Canals Riera. Director Tecno-med Ingenieros y Claire Murphy. Socio Consultor Tecno-med Ingenieros ![]()
No te pierdas este evento, esperamos poder saludarte allí.


#COVID19 FAQ regulatorias – ¿Que requisitos tienen las neveras y congeladores para vacunas COVID19? Son producto sanitario? hay normativa?
Una pregunta que nos han realizado ultimamente desde importadores, distribuidores y centros sanitarios es la relativa a requisitos regulatorios de los frigorificos y congeladores. Estos productos en la legislación actual Directivas 93/42 y 98/79/CE sólo contempla los destinados a bolsas de sangre y plasma que son de la clase IIa precisando sólo estos para su marcado CE la intervención de un Organismo Notificado. Son para su uso en un banco de sangre y centros sanitarios, uso profesional. read more…

Jornada «Regulacion productos sanitarios FDA» by @FENIN_es 2 marzo 2021 – 10h-12h30
No os perdáis esta jornada donde tendremos la presentación de los requisitos de la FDA para los productos sanitarios. Participa David Salvatierra Director de Calidad y PRCN de Leventon, uno de los mayores expertos españoles de productos sanitarios y con una dilatada experiencia en su presentación e inspección por la CDRH de la FDA.
A las empresas con productos sanitarios que vayais a exportar a UDA os recomendamos si aun no estáis asociados a FENIN que lo hagáis cuanto antes.
Visita su web ¿Como asociarse?

Formacion «Electromedicina, equipos analizadores de IVD e implantables activos segun MDR e IVDR» en el curso de posgrado «Experto Productos Sanitarios» 2020 @UniBarcelona
Este año vía webinar, no te pierdas esta formación si quieres ser PRCN con los nuevos reglamentos MDR e IVDR
Con la participación de Claire Murphy y Xavier Canals de Tecno-med Ingenieros como parte del equipo de profesores.
mas información: http://www.ub.edu/tecnofarm/tecnologia/masters-i-postgraus

Foro de Inversión Healthcare Barcelona 24 Marzo 2021 by @COMBarcelona @Biocat_cat @BarcelonaActiva @ESADE
El Foro de Inversión Healthcare Barcelona es un punto de encuentro entre emprendedores e inversores del sector sanitario. Se pueden presentar todo tipo de empresas con proyectos de Biotecnología, productos sanitarios, Servicios sanitarios y Tecnologías de la Información relacionadas con la salud. El Foro de Inversión Healthcare Barcelona se ha posicionado como referente en el ecosistema biomédico, promoviendo la innovación y el emprendimiento entre el colectivo con el objetivo de acercar emprendedores e inversores del sector sanitario participando en el mismo los actores principales motores de innovación de Barcelona. ![]()
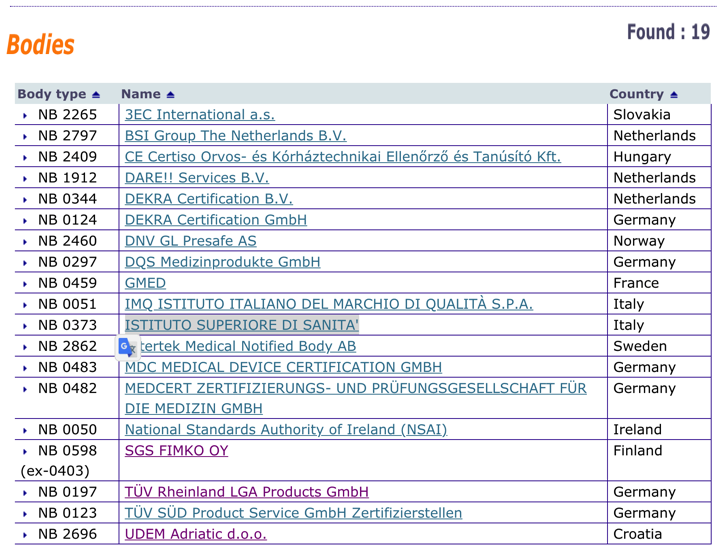
Organismos Notificados: ISS (Italia) ON num. 0373 nuevo ON con MDR. Enhorabuena!!!
Nueva designación del Organismo Notificado ISS ISTITUTO SUPERIORE DI SANITA,
Viale Regina Elena, 299 00161 – ROMA – Italy
Phone : +39 06 49906146 Fax : +39 06 49903150 mail : roberta.marcoaldi@iss.it Web: www.iss.it
es el homologo italiano de la AEMPS
Feria @Arab_Health 2021 – 21 a 24 Junio 2021 (23 Mayo a 22 Julio online)
RMD 2021 EAAR Annual Conference on New Medical Device Regulations con la participación de @tecno_med
Gran asistencia de empresas del sector al webinar @FENIN_es de productos sanitarios anexo XVI con @AEMPSgob, ON0318, CERE y @tecno_med
 En esta jornada donde estaban prácticamente todos los técnicos del sector, Maria Alaez y los expertos de la AEMPS nos contaron la última hora del reglamento MDR en lo que respecta a los productos de anexo XVI. Pensamos que pronto pues se va a poder abrir el grupo del sector de medicina estética.
En esta jornada donde estaban prácticamente todos los técnicos del sector, Maria Alaez y los expertos de la AEMPS nos contaron la última hora del reglamento MDR en lo que respecta a los productos de anexo XVI. Pensamos que pronto pues se va a poder abrir el grupo del sector de medicina estética.
Tuvimos el honor de participar Claire Murphy y Xavier Canals de Tecno-med para contar como se clasifican los productos de este anexo y como se establece su documentación técnica y sistema de calidad.
A las empresas con productos afectados por este anexo os recomendamos si aun no estáis asociados a FENIN que lo hagáis cuanto antes ….
Visita su web ¿Como asociarse?
No Results Found
The page you requested could not be found. Try refining your search, or use the navigation above to locate the post.
Nueva guía de FDA para EMC sustituye a la de 2016 @FDAdeviceInfo se aplica a partir de agosto de 2022 y de junio 2023 para IVDs
FDA indica en el alcance del documento que se aplica a productos sanitarios incluyendo a los productos sanitarios para diagnóstico in vitro. Hace referencia a las familias de normativa IEC 60601 / 80601 y a la IEC 601010-1 para IVD.
Nos da un listado, de A a K, de información que debemos incluir en nuestro 510k: read more…

La CAMD publica una declaración sobre el estado de los Reglamentos (menos mal que las Autoridades Sanitarias tienen mas sentido común que los políticos)
El grupo de Autoridades Competentes para los productos sanitarios ha publicado esta declaración, que nos da esperanza en que podamos tener una transición mas o menos ordenada (os la hemos traducido para facilitar su difusión): read more…

nueva norma IEC TR 60601-4-5:2021 de ciberseguridad de equipos electromédicos
Nueva norma de la serie 60601que esta dirigida a la ciberseguridad de productos sanitarios utilizados en redes IT medicas. 
Adhiérete a nuestro contrato de vigilancia tecnológica y estarás al día de las novedades normativas y reglamentarias. No más sorpresas, entérate antes de que sea una no conformidad. https://www.meddev.biz/b2c/producto/WEB105/1/vigilancia-tecnologica-productos-sanitarios
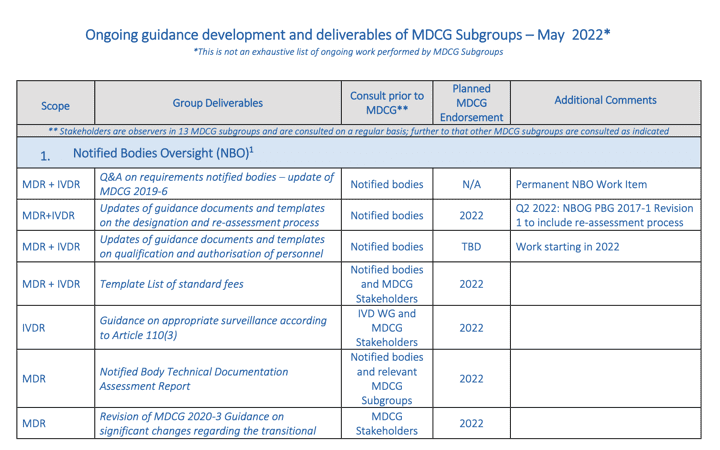
MDCG (Grupo de Coordinación de Productos Sanitarios) publica la lista de guías en curso

MDCG: nueva MDCG 2022-10 Q&A relativo a la interfase entre el reglamento 536/2014 de ensayos clínicos de medicamentos e IVDR

Hoy 26 de Mayo de 2022 es la fecha de aplicación del Reglamento (EU) 2017/746 de Productos Sanitarios para Diagnóstico in Vitro
Como ya estaba establecido en el texto original que entró en vigor el 26 de mayo de 2017, hoy termina el periodo transitorio y entra en aplicación el Reglamento IVDR.
Consulta sobre la adecuación de la documentación que avala la conformidad de una familia de producto sanitario IVD legacy
![]()
pide nuestra asesoría en la 4-0175 Adaptación ps LEGACY IVDD a periodo de gracia

Publicada nueva lista de normas armonizadas con MDR – Decision de Ejecución (UE) 2022/757 incluyendo la EN ISO 14971
Como ya nos anunció Mario Gabrielli Cossellu (Legal and Policy Officer at European Commission) en su participación que tuvimos el placer de seguir en RAPS Euroconvergence de Amsterdam.
Se modifica la entrada de norma 10 para incluir la modificación intermedia:
10. EN ISO 13485:2016 Productos sanitarios. Sistemas de gestión de la calidad. Requisitos para fines reglamentarios. (ISO 13485:2016).
EN ISO 13485:2016/AC:2018
EN ISO 13485:2016/A11:2021
es decir en nuestra lista de normas hemos de incluir:
10. EN ISO 13485:2016 + /AC:2018 + /A11:2021
y se incluyen:
15. EN 285:2015+A1:2021 Esterilización. Esterilizadores de vapor. Esterilizadores grandes.
es decir en nuestra lista de normas hemos de incluir:
15. EN 285:2015+A1:2021
16. EN ISO 14971:2019 Dispositivos médicos/productos sanitarios (MD). Aplicación de la gestión de riesgos a los MD. (ISO 14971:2019).
EN ISO 14971:2019/A11:2021
es decir en nuestra lista de normas hemos de incluir:
16. EN ISO 14971:2019 + /A11:2021![]()

SBA Sterile Barrier Association publica la guía de los símbolos usados en MDR e IVDR según la ISO 15223-1 para los envases estériles
La asociación SBA, Sterile Barrier Association ( https://sterilebarrier.org/ ), ha publicado una guía donde podemos ver símbolos relativos al envasado estéril para el etiquetado e instrucciones de uso según la nueva edición de la ISO 15223-1.Es muy útil la tabla para la correcta apertura de los distintos envases.