En este documento se responde a las siguientes preguntas:
Pregunta 1: ¿Cuál es el marco regulatorio aplicable para dispositivos médicos y equipos de protección personal en la UE?
Pregunta 2: ¿Cómo se puede colocar legalmente un producto en el mercado de la UE?
Pregunta 3: ¿Pueden ser válidos otros documentos para colocar legalmente un producto en el mercado de la UE?
Pregunta 4: ¿Cuáles son las características principales de una declaración de conformidad válida?
Pregunta 5: ¿Cuáles son las principales características de un certificado válido?
Pregunta 6: ¿Cuándo se requiere la intervención de un organismo notificado?
Pregunta 7: ¿Puede un informe de prueba de acuerdo con una norma permitir la comercialización de un producto en la UE?
Pregunta 8: ¿Son posibles las excepciones a los requisitos legales (por ejemplo, productos sin la marca CE o sin una declaración de conformidad), en particular en el contexto de la pandemia de COVID-19?
Pregunta 9: ¿Dónde se puede encontrar información más detallada sobre el marco regulatorio de la UE aplicable?
Tened en cuenta además los requisitos específicos para España que en el caso de productos sanitarios nos requiere la licencia de fabricante o importador, las comunicaciones de distribuidor y el registro en la base de datos RPS o CCPS.
Así para el caso de mascarillas, tenemos los dos casos y el caso de «dual» en que deben cumplirse ambas:
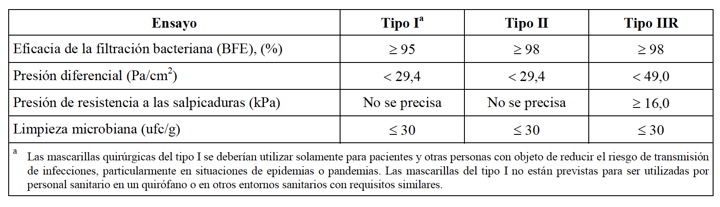
1. mascarillas quirúrgicas
norma EN 14683 Mascarillas quirúrgicas – Requisitos y métodos de ensayo
NO precisan de intervención de Organismo Notificado
Es una buena práctica también solicitar el certificado de ensayo según la norma EN 14683 con la eficacia del filtro.
2. respiradores – medias mascaras filtrantes – norma EN 149
AITEX Judit Sisternes jsisternes@aitex.es el 965542200
INSST https://www.insst.es/-/servicios-que-ofrece-el-cnmp-como-organismo-notificado
CENTRO NACIONAL DE MEDIOS DE PROTECCION DEL INSHT (CNMP) Sevilla
tel 954514111 pcaceres@insht.meyss.es